亚博 细胞的“命悬一线”或由它掌控 | 科技前哨
发布日期:2026-04-09 00:23 点击次数:169

细胞的存活与弃世受到精密的分子信号网罗调控。肿瘤坏死因子受体1(TNFR1)手脚病笃的多服从跨膜受体,恰是其中的要道“调控开关”。它介导的信号通路,在细胞弃世、炎症和免疫反映中弘扬要道作用,而其在胞内的信号复合物(复合物I)的动态聚首妥协离,会在十几分钟内决定细胞生死。经久以来,这一复合物在TNFR1受到细胞外配体TNF激活后,快速拼装妥协体的启动机制遥远是TNFR1限度的病笃未解之谜。
日前,中国科学院上海有机化学探求所探求团队,揭示了电偶极矩作用劲启动TNFR1通路复合物I的动态变化机制,为学界相识细胞信号调控机制提供了全新视角。
01
捕捉中枢 “真面孔”
探求团队领先通过实际,得胜捕捉到复合物I的中枢结构,并用冷冻电镜技巧解析了其高分辨率结构。
结构分析泄露,该中枢是由TNFR1、TRADD和RIPK1的31个弃世结构域单位构成的螺旋型超大复合物,它们有序摆列为6层五聚体,亚博体彩酿成典型的螺旋型纤维结构。
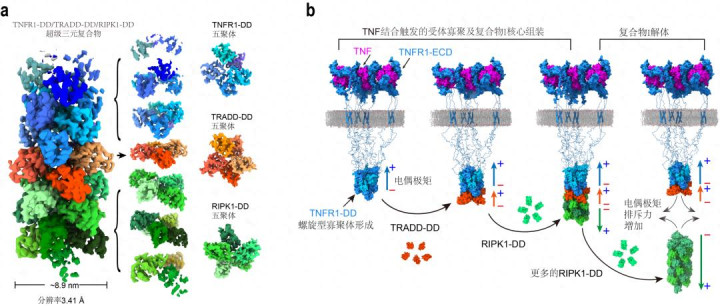
TNFR1信号复合物动态拼装妥协体的机制图
该复合物的结构特征特殊显明:5个TRADD弃世结构域领先拼装成一个五聚体中枢,其凹凸名义辨别聚首了两层TNFR1和RIPK1五聚体。
结构分析和突变体功能探求标明,来自TNFR1、TRADD和RIPK1的三类弃世结构域通过精湛互补的静电名义,酿成特异性互相作用,最终拼装成高度有序的螺旋型复合物。
这一明晰的结构图谱,让探求团队得以从分子层面,进一步探索复合物I拼装与解体的内在驱能源。
02
变化的 “隐形推手”
探求团队聚首结构分析、突变体功能探求和计较分析,找到了启动复合物I动态变化的 “隐形推手”——电偶极矩作用劲。
计较分析发现,三种弃世结构域酿成的螺旋型纤维名义,存在渊博正负电荷高度分离的特征,这使得三种弃世结构域寡聚体之间酿成了显着的云尔电偶极矩互相作用。而这一互相作用的标的,恰是决定复合物I拼装与解离的要道。
该探求初度发现了电偶极矩之间的长程互相作用在细胞信号转导中的病笃生物学功能亚博,阐发了TNFR1复合物I快速拼装又精确解离的动态举止,对揭示细胞弃世与存活的分子开关机制具有病笃真谛。
凤凰彩票官网首页 - Welcome